Paul Bilars, ceo.
VarmX, de biotechonderneming die een medicijn ontwikkelde voor patiënten met antistollingsmiddelen om te voorkomen dat ze aan acute bloedingen overlijden, heeft € 12,5 miljoen financiering opgehaald. € 7,5 miljoen werd geïnvesteerd door InnovationQuarter Capital en BioGeneration Ventures (BGV) en de Rijksdienst voor Ondernemen (RVO) vulde de financiering aan met € 5 miljoen innovatiekrediet. Met behulp van de financiering wordt de ontwikkeling van het medicijn richting de klinische studies aanzienlijk versneld.
Verbale en performale intelligentie ontmoeten elkaar in het duo Pieter Reitsma en Paul Bilars: de een is wereldwijd gerenommeerd wetenschapper op het gebied van bloedstolling, de ander was manager bedrijfsvoering in het LUMC. De een doet het technische denkwerk, de ander het operationele. Inmiddels hebben ze allebei een andere baan. Samen leiden ze VarmX, een spin-off-onderneming van het LUMC. Onder die vlag proberen ze het door emeritus hoogleraar Pieter Reitsma uitgevonden medicijn – PseudoXa – op de markt te brengen. En dat is geen sinecure; succesvol een medicijn op de markt brengen lukt niet veel bedrijven. Je moet er ontzettend veel geld in steken en tot het getest is op mensen, kun je nauwelijks inschatten of het echt goed werkt. Maar als het wél lukt, heb je een medicijn in handen dat voorkomt dat patiënten met antistollingsmedicijnen overlijden door een niet te stelpen bloeding. Voor VarmX staan de sterren voorlopig gunstig. Het geheim? Eindeloos toetsen bij experts, die experts weer laten toetsen door andere experts en tenslotte een alles-doorklievende ambitie.
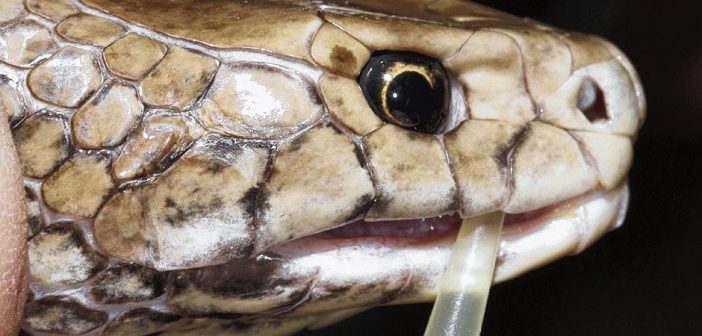
Drie jaar geleden stapte Pieter Reitsma, inmiddels emeritus hoogleraar moleculaire en experimentele geneeskunde bij het LUMC, het kantoor van Paul Bilars binnen. Hij had een stukje DNA uit slangengif gehaald en er een medicijn mee gemaakt dat de werking van de nieuwe generatie antistollingsmiddelen tegengaat. Zo’n 2 à 3 procent van de patiënten met dat type antistollingsmedicijnen overleed nu namelijk aan acute bloedingen of op de operatietafel. “Als manager bedrijfsvoering had ik vaker te maken met intellectueel eigendom en uitvindingen,” vertelt Paul Bilars. “Maar wat Pieter me toen vertelde, klonk bijna als science fiction. Slangengif als inspiratie voor medicijnen, dat was echte innovatie. Dit moet de markt op, zei ik.”
PseudoXa: wat is het?

Pieter Reitsma
Normaal gesproken vraagt slangengif om een medicijn, maar het team van Pieter Reitsma en Mettine Bos van het LUMC maakte ván slangengif een medicijn. Gif van de Australische bruine slang om precies te zijn – na de inland taipan de giftigste slang ter wereld. Het gif van de bruine slang doet het bloed van zijn prooi stollen en veroorzaakt zo een zuurstoftekort. Een van de eiwitten die een rol spelen bij die bloedstolling (Factor X, waarbij de X een Romeinse tien is) bleek in de slangenvariant een langer lusje te bevatten dan hetzelfde eiwit bij mensen. Daardoor bindt het slangeneiwit minder goed aan de antistollingsmiddelen en wordt de werking ervan opgeheven. Dat kan bijvoorbeeld nodig zijn als een trombosepatiënt met antistollingsmedicijnen geopereerd moet worden. Om te voorkomen dat hij op de operatietafel doodbloedt door de bloedverdunners, kan dan een injectie PseudoXa toegediend worden. Reitsma: “Het bloed stolt dan weer normaal zonder dat het risico op bloedpropjes extra verhoogd wordt – het is dan weer even hoog als voor het medicijngebruik.” Reitsma besloot slechts die langere lus uit het slangeneiwit op te nemen in het menselijk eiwit en noemde het PseudoXa. In deze variant zorgt het eiwit wel voor stolling, maar woekert het niet als een gif.
De markt op: zoek een partner in crime
Een medicijn uitvinden is één ding, het op de markt brengen een tweede. “Er was ons geadviseerd ons verhaal tegen InnovationQuarter aan te houden, omdat alle expertise om je bedrijf opgeschaald te krijgen in één organisatie zit. Business developers en investeerders uit verschillende fondsen praten daar voortdurend met elkaar. En het zakelijke netwerk reikt tot diep in de provincie, zowel in overheid als bedrijfsleven. Bovendien heeft InnovationQuarter een profiel als lifecycle financier,” zegt Paul Bilars. “Voor het ontwikkelen en op de markt brengen van medicijnen heb je namelijk in de diverse stadia van medicijnontwikkeling geld nodig – vele miljoenen. In de allervroegste fase is het vinden van geldschieters bijzonder moeilijk. Investeerders zien liever dat zo’n medicijn eerst een aantal keer in muizen zijn werkzaamheid heeft bewezen, voordat ze het pas aandurven er geld in te steken.”
Toch had VarmX al een seed ronde binnen weten te halen van € 250.000 bij het Universiteit Leiden Fonds. Maar dat fonds ging op in het vroege-fasefonds UNIIQ. “We hebben er toen voor gekozen ons voorstel alsnog bij UNIIQ in te dienen, omdat het netwerk van InnovationQuarter belangrijk voor was,” zegt Bilars. Het voorstel werd geaccepteerd en bezorgde VarmX de eerste investering van € 300.000. Een jaar later volgde een tweede investering van IQ Capital en BioGeneration Ventures van € 1 mln. En onlangs deed InnovationQuarter een derde investering in VarmX samen met BioGeneration Ventures en RVO. En die laatste ronde leverde maar liefst € 12,5 mln. op.
Goede kansen voor VarmX
Omgekeerd was VarmX voor InnovationQuarter ook een interessant partij. “Veel wetenschappers zitten vooral in het laboratorium en hebben weinig kaas gegeten van hoe je een uitgevonden medicijn verkoopt,” zegt René Brama van IQ Capital. “Maar Pieter Reitsma stond altijd al met een half been in de farmaceutische markt. We hebben uit zijn netwerk kunnen putten bij het samenstellen van de Raad van Advies. Daar zitten nu dus echt wereldspelers uit de wetenschappelijke en farmaceutische industrie tussen. De big farma’s kijken mee wat hier ontwikkeld wordt. En dat maakt de succeskansen voor VarmX een stuk groter dan de gemiddelde academische spin-off.”
Hoe ontwikkel je een medicijn?
Om medicinale eiwitten te kunnen produceren, wordt gebruikt gemaakt van zogenaamde cellijnen. Die cellijnen zijn in laboratoria gestabiliseerd, doorgekweekt en onsterfelijk gemaakt en worden als basis gebruikt voor medicijnontwikkeling. In het geval van PseudoXa was de cellijn afkomstig uit de eierstok van een Chinese hamster. Deze zogenaamde CHO-lijn, Chinese Hamster Ovary cells (CHO) zijn door de EMA en FDA goedgekeurd. Het extra lusje eiwit uit het slangengif wordt in de DNA code voor menselijk stollingsfactor X gebouwd en dan in de hamstercellijn geïmplanteerd. Het nieuwe eiwit dat dan gemaakt wordt door de CHO-cellen, is inmiddels gepatenteerd en heet nu PseudoXa.
Als je de cellijn eenmaal hebt ontwikkeld, is het zaak die cellen op steeds grotere schaal te kweken, tot in vaten van 100 liter of meer. In het geval van PseudoXa is de cellijn in Zwitserland ontwikkeld. Met behulp van de eerdere investering van € 1 mln. is er 4 gram PseudoXa geproduceerd. Met behulp van de investering van € 12,5 mln. wordt er nu een batch van 1000 liter geproduceerd. De rest van de € 12,5 mln. is voldoende om PseudoXa via dierproeven en testen op vrijwilligers tot aan de clinical trials te brengen. In dat laatste stadium wordt het medicijn in een grootschalige studie op patiënten in ziekenhuizen en eerste hulpposten getest
De kracht van een dreamteam
De kracht van VarmX ligt bovendien in het veelvuldig sparren met experts. “Een medicijn ontwikkelen betekent voortdurend beslissingen moeten nemen in een volatiel, grijs gebied en in een keiharde markt,” vertelt Paul Bilars. “Dan kun je het je niet veroorloven om zelf te gaan googelen, maar moet je je omringen met een netwerk van experts. Gelukkig hebben we mede dankzij Pieter toegang tot zo’n netwerk.” Paul vertelt dat hij en Pieter het Drug Development Plan, uitbesteed aan een consultant, nog eens extra hebben laten doorspitten door een tweede consultant. “Daarvoor zijn we zelfs naar Boston afgereisd,” vertelt Pieter Reitsma. “We willen blijven checken of de partijen waarmee we werken echt de expertise in huis hebben om dit medicijn op de markt te krijgen. Gelukkig was de eerste opmerking in de feedback: wat een verrekte goed plan is dit.”
Ook een krachtige commitment en het vermogen je ego opzij te zetten, zijn onontbeerlijk. “Er zijn scenario’s denkbaar waarin bijvoorbeeld de technische kennis van Pieter niet meer nodig zal zijn voor VarmX. Of waarin er een meer ervaren biotech-CEO aangetrokken wordt om het bedrijf te gaan leiden,” zegt Bilars. “Dan is het aan ons om zo’n besluit niet persoonlijk op te vatten. Samen hebben wij maar één droom: PseudoXa op alle eerste hulpposten en in ziekenhuizen krijgen. Deze twee mannen zijn slechts een voertuig.”
Beter dan de concurrent
De concurrent van VarmX heeft als eerste een tegenmedicijn voor de DOAC’s op de markt gebracht: Andexxa. “Andexxa heeft echter de bijwerking dat het bij toediening het risico op trombose verhoogt, terwijl het tromboserisico bij PseudoXa gelijk blijft ten opzichte van het risico van voor het gebruik van de DOAC’s,” zegt Pieter Reitsma. “Bovendien zijn de kosten voor Andexxa heel erg hoog. Bijna perverse prijzen. Wij hopen PseudoXa tegen veel lagere kosten te kunnen produceren.”
Toch is het niet verwonderlijk dat Andexxa de markt heeft gehaald. “Dit type medicijn noemen ze ‘weesmedicijnen’,” zegt René Brama van IQ Capital. “Als er tegen zeldzame aandoeningen nog geen medicijn bestaat, dan hanteert de overheid het principe: beter iets dan niets. Er geldt dan een lichter traject om je medicijn op de markt te krijgen. Dat maakt de kansen voor VarmX wederom groter, want ook PseudoXa kan in die verlichte procedure mee.”
In 2019 wordt het eerste honderd-litervat PseudoXa gebrouwen. Wat drie jaar geleden in een ziekenhuis begon, gaat dan volwassen vormen aannemen. In 2022 verwachten de Leidse heren de markt op te kunnen met PseudoXa. En dan is science fiction werkelijkheid geworden.
Bron: InnovationQuarter